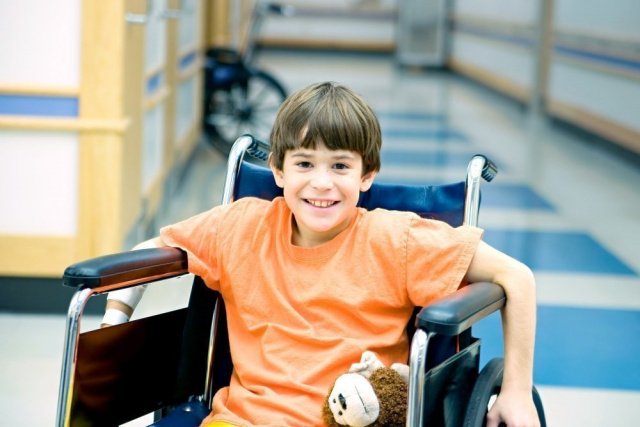
7 сентября — международный день распространения информации о синдроме Дюшенна. Это одна из самых часто встречающихся наследственных генетических патологий — диагностируется она у одного из 3000 новорожденных мальчиков. Пока что способов полного излечения от болезни не существует, но новые разработки дают шанс изменить ситуацию. Какой может быть терапия будущего, расскажет MedAboutMe.
Что такое мышечная дистрофия Дюшенна?

Мышечная дистрофия Дюшенна — наследственная генетическая патология, одна из тех, которые поражают только мальчиков. Болезнь передается от матерей, но сами женщины от нее не страдают, а являются здоровыми носителями пораженного гена. Ген может передаваться по женской линии многие поколения и никак не проявляться, поэтому рождение ребёнка с дистрофией Дюшенна для семьи часто становится неожиданностью.
Патология заключена в гене, кодирующем белок дистрофин — при болезни он вырабатывается в недостаточном количестве или вовсе отсутствует. А поскольку дистрофин является основой мышечных волокон, у детей с дистрофией Дюшенна мышцы постепенно ослабевают, перерождаются и заменяются жировой или соединительной тканью. Это приводит к инвалидизации — болезнь неуклонно прогрессирует, постепенно захватывает все больше мышц.
Даже с существующим сегодня лечением мальчики с миодистрофией Дюшенна живут в среднем 20-25 лет. В некоторых случаях больные доживают до 40, но пока это все же исключение, чем правило.
Первые симптомы болезни возникают еще до 3 лет, в этом возрасте у ребёнка проявляется:
- быстрая утомляемость;
- отставание в развитии;
- трудности с освоением навыка ходьбы, дети часто ходят на пальчиках;
- симптом Говерса — при попытке встать ребёнок активно помогает себе руками, поскольку мышцы ног уже не справляются.
Болезнь прогрессирует, и уже у больных 15-18 лет наблюдаются следующие признаки:
- деформация скелета;
- неспособность передвигаться без инвалидного кресла, вставать, самостоятельно сидеть, иногда даже двигать руками;
- эндокринные расстройства отмечаются у 30-50% больных;
- поражение сердечной мышцы, кардиомиопатия;
- поражение дыхательной мускулатуры;
- иногда встречаются нарушения психического развития.
На том этапе, когда болезнь захватывает сердце и легкие, помочь пациенту уже практически невозможно.
Стандартные методы лечения

Болезнь была описана еще в XIX веке неврологом Гийомом Дюшенном, в честь которого она и названа. И с того времени врачи ищут эффективные способы терапии. Первым методом, который используется до сих пор, стало применение ортопедических устройств.
Тренировка мышц помогает немного замедлить процесс их разрушения. Для пациентов применяется как активная (пока они сами в состоянии заниматься), так и пассивная тренировка. Врачи отмечают, что регулярные упражнения способны продлить период, когда пациент передвигается без инвалидной коляски.
По статистке, практически половина больных миодистрофией переживают операцию на позвоночнике. При слабых мышцах скелет искривляется, что существенно ухудшает течение болезни. Поэтому на помощь таким больным приходят различные ортопедические приспособления — фиксация костей и суставов позволяет замедлить их деформацию.
Современные разработки в этом направлении терапии давно вышли за пределы простых поддерживающих средств. Так, разработанная нидерландским Университетом Твенте роботизированная рука A-Gear способна заменить человеку атрофированную конечность. Искусственная рука улавливает электрические сигналы от мышц или минимальное мышечное напряжение. Люди с миодистрофией Дюшенна могут управлять механической конечностью, движения при этом получаются очень точными и естественными. «К исследованию мы привлекли много участников, которые уже на протяжении 3-5 лет утратили способность двигать руками, — говорит ученый Джоан Лобо-Прат (Joan Lobo-Prat). — A-Gear помогла им частично вернуть функциональность конечностей».
Лекарства при миодистрофии Дюшенна

Медикаментозное лечение является важной частью общей терапии. Наиболее популярной группой препаратов для пациентов с миодистрофией Дюшенна являются стероиды: преднизолон, дефлазакорт и другие. Начинают их прием еще в возрасте 4-6 лет, когда проявляются признаки болезни, но существенного ухудшения состояния нет. Стероиды помогают отсрочить развитие тяжелых симптомов, но в долгосрочной перспективе они неэффективны. Как только у пациента начинает прогрессировать атрофия, улучшить состояние мышц эти лекарства уже не могут. И все же стероиды остаются важной составляющей лечения дистрофии Дюшенна.
Существуют и другие разработки, направленные на улучшение работы мышц. Так, в 2016 году FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) одобрило лекарство Exondys51 (этиплирсен), которое сможет стать конкурентом стероидам. По данным проведенных исследований, вещество способно укрепить мышечную ткань, ведь оно увеличивает уровень дистрофина в скелетных мышцах. Однако не все врачи разделяют мнение FDA, поскольку утверждение препарата проходило по ускоренной процедуре. По факту сейчас нет однозначных доказательств, что он может отсрочить развитие паралича или ослабить симптомы развитого заболевания. А значит, Exondys51, как и стероиды, проявляет эффективность лишь в коротком периоде болезни. Несмотря на то, что лекарство уже утверждено, FDA продолжает исследования. Если эффективность препарата не будет подтверждена, его производство остановят.
Европейский Комитет по лекарственным препаратам для человека (CHMP) в 2014 году зарегистрировал другой медикамент — Трансларна (аталурен). В отличие от других лекарств, которые только укрепляют мышцы, аталурен способен восстанавливать нарушенный синтез белков. А значит, теоретически устраняет саму причину развития болезни. Поскольку это новая разработка, понять, насколько она эффективна в долгосрочной перспективе, пока трудно. Но промежуточные результаты достаточно обнадеживающие.
Редактирование генома и технология CRISPR/Cas

Миодистрофия Дюшенна вызвана патологией в гене, поэтому любое медикаментозное или физиотерапевтическое лечение является всего лишь симптоматическим. Вылечить человека можно только с помощью генной терапии — редактирования кода ДНК и изменения «больного» гена. Несмотря на то, что пока такое лечение не применяется, новые технологии дают шанс на решение проблемы в будущем.
В последнее время особую популярность получила технология CRISPR/Cas9. В ее основе — действие специального фермента Cas9. Он внедряется в клетку и там способен не только распознавать конкретный участок ДНК-цепочки, но и удалять его. Поскольку врачи знают, какой ген виноват в развитии болезни и где конкретно он находится, с помощью технологии они смогут просто вырезать фрагмент ДНК с патологией. А это принесет полное выздоровление.
Однако недавние исследования выявили ряд трудностей с использованием этой системы. После проведенного эксперимента на эмбрионах оказалось, что метод действительно позволил вылечить до 30% клеток. Но при этом такое внедрение породило большое количество других мутаций.
Возможности CRISPR/Cas9 активно изучают многие лаборатории мира. Положительные результаты, в частности, получили ученые из Юго-западного медицинского центра Техасского университета. Здесь CRISPR/Cas9 успешно применили для лечения мышей с миодистрофией Дюшенна. Также была разработана более точная технология, подходящая именно для этой болезни — в ней белок Cas9 был заменен белком Cpf1. «Мы взяли у пациентов с дистрофией Дюшенна клетки и смогли исправить их в лабораторных условиях, — говорит доктор Эрик Олсон. — После применения CRISPR/Cpf1 в клетках восстановилось производство дистрофина».
Другие исследования: искусственная хромосома, вирусы и мутации

Группа японских и британских ученых предложила еще один альтернативный подход для лечения миодистрофии Дюшенна — внедрение искусственных здоровых хромосом (ген с патологией находится в Х-хромосоме 23-й пары). Такая хромосома будет помещена в стволовую клетку, а позже введена в организм и поможет восстановить мышцы. Пока положительные результаты получены в опытах на мышах. Похожие исследования проводились и в России, в Институте стволовых клеток человека.
Еще одно возможное направление в лечении болезни Дюшенна появилось благодаря собаке. Более десяти лет назад ученые из Университета Сан-Паулу в Бразилии специально для изучения выводили щенков с мышечной дистрофией Дюшенна. Однако, несмотря на подтвержденный анализами диагноз, у одного из них, пса Ринго, заболевание не развилось, более того, животное прожило 11 лет без каких-либо симптомов. Ученые связывают это с наличием у собаки другой патологии — мутации в гене Jagged1. «Мы точно не знаем, какова должна быть концентрация белка, который кодируется геном Jagged1, в мышцах, чтобы эффективно защищать от развития болезни, — рассказывает генетик Луис Канкел. — Но история Ринго наталкивает на мысль, что мутация Jagged1 компенсирует атрофию, вызванную нехваткой дистрофина».
Одной из самых обнадеживающих перспектив является масштабное исследование, в котором примут участие реальные пациенты. Суть эксперимента — попробовать внедрить в клетку исправленную копию гена дистрофина. И сделать это планируется с помощью вирусов — именно они станут переносчиками нужного фрагмента ДНК. Испытания будут проводиться в США уже в конце 2017-начале 2018 года. В частности, в исследованиях будет участвовать фармацевтическая компания Pfizer. Пока отобрано 12 детей разных возрастных групп, которым в детской больнице Nationwide штата Огайо будут введены вирусные частицы.