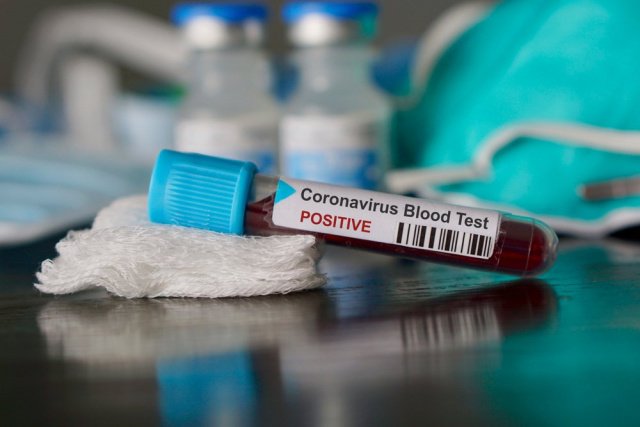
Вчера, 4 февраля, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) в экстренном порядке разрешило массовое использование нового диагностического теста, позволяющего выявлять людей, инфицированных коронавирусом из Уханя 2019-nCoV.
Пока тест будет использоваться только в 200 лабораториях страны, авторизованных Центрами по контролю и профилактике заболеваний (CDC). В основе теста лежит метод полимеразной цепной реакции в реальном времени (RT-PCR). Применяться он будет не ко всем пациентам подряд с симптомами ОРВИ, а только к тем, которые соответствуют критериям CDC для проверки на коронавирус.
Появление теста для выявления 2019-nCoV особенно актуально на фоне растущего числа американцев, зараженных новым вирусом. На данный момент в США подтверждено 11 случаев заболевания, 167 обследованных показали отрицательный результат, 82 человека проходят обследование и 36 находятся под наблюдением экспертов CDC.
Только 1 из 11 случаев заражения в США был выявлен в ходе проверки в аэропорту. Еще 1 случай был обнаружен при проверке близких контактов зараженного человека. Остальные 9 больных были выявлены врачами, не относящимися к CDC. Это позволяет надеяться, что при распространении теста по стране процесс обнаружения людей с новым коронавирусом пойдет быстрее.
Эксперты подчеркивают, что отрицательный результат теста не исключает полностью заражение новым коронавирусом и не должен использоваться в качестве единственного основания для назначения лечения и других действий в отношении пациента.